Analyse de la Dualité Onde-Particule
Contexte : Le paradoxe au cœur du monde quantique.
La physique quantique a bouleversé notre compréhension de la réalité en révélant que les objets microscopiques, comme les électrons, ne se comportent ni comme des billes (particules) ni comme des vagues (ondes), mais présentent les deux aspects à la fois. C'est la dualité onde-particulePrincipe fondamental de la mécanique quantique qui stipule que tout objet physique peut présenter simultanément des propriétés d'ondes (comme la diffraction) et de particules (comme une position localisée).. L'expérience des fentes de Young, réalisée avec des électrons, en est l'illustration la plus célèbre et la plus déroutante. Cet exercice vous propose d'analyser quantitativement ce phénomène en calculant les propriétés ondulatoires d'un électron à partir de ses caractéristiques corpusculaires.
Remarque Pédagogique : Cet exercice est une porte d'entrée vers les concepts fondamentaux de la mécanique quantique. Nous allons lier l'aspect "particule" d'un électron (son énergie cinétique, sa quantité de mouvement) à son aspect "onde" (sa longueur d'onde et les figures d'interférence qu'il produit). C'est une démarche essentielle pour comprendre comment les physiciens modélisent le monde à l'échelle atomique.
Objectifs Pédagogiques
- Calculer la quantité de mouvement d'un électron à partir de son énergie cinétique.
- Appliquer l'hypothèse de De Broglie pour déterminer la longueur d'onde associée à une particule.
- Utiliser la formule des interférences d'Young pour prédire l'espacement des franges.
- Se familiariser avec les constantes fondamentales (Planck, masse de l'électron) et les unités du monde quantique (eV, nm, kg·m/s).
Données de l'étude
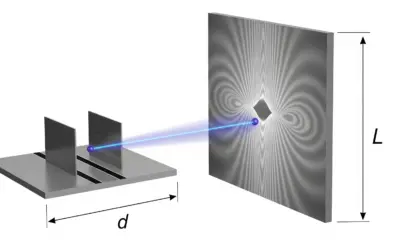
Schéma de l'expérience des fentes de Young avec des électrons
| Paramètre / Constante | Symbole | Valeur | Unité |
|---|---|---|---|
| Énergie cinétique de l'électron | \(E_c\) | 150 | \(\text{eV}\) |
| Distance fentes-écran | \(L\) | 1.0 | \(\text{m}\) |
| Écartement entre les fentes | \(d\) | 50 | \(\mu\text{m}\) |
| Masse de l'électron | \(m_e\) | 9.11 x 10-31 | \(\text{kg}\) |
| Constante de Planck | \(h\) | 6.626 x 10-34 | \(\text{J} \cdot \text{s}\) |
| Charge élémentaire | \(e\) | 1.602 x 10-19 | \(\text{C}\) |
Questions à traiter
- Convertir l'énergie cinétique de l'électron en Joules, puis calculer sa quantité de mouvement \(p\).
- Calculer la longueur d'onde de De Broglie \(\lambda\) associée à cet électron.
- Calculer l'interfrange \(\Delta y\) (distance entre deux franges brillantes consécutives) sur l'écran.
- Calculer l'angle \(\theta_1\) de la première frange brillante (k=1) par rapport à l'axe central.
Les bases de la Dualité Onde-Particule
Avant la correction, rappelons les idées révolutionnaires qui sous-tendent cet exercice.
1. L'Énergie Cinétique (Aspect Particule) :
Classiquement, un objet de masse \(m\) et de vitesse \(v\) possède une énergie cinétique \(E_c = \frac{1}{2}mv^2\). Sa quantité de mouvement est \(p = mv\). On peut relier les deux sans passer par la vitesse :
\[ p = \sqrt{2 \cdot m_e \cdot E_c} \]
Cette formule est la base pour décrire l'aspect corpusculaire de l'électron.
2. L'Hypothèse de De Broglie (Le Pont Onde-Particule) :
En 1924, Louis de Broglie postule que toute matière en mouvement est associée à une onde. La longueur d'onde \(\lambda\) de cette "onde de matière" est inversement proportionnelle à la quantité de mouvement \(p\) de la particule :
\[ \lambda = \frac{h}{p} \]
où \(h\) est la constante de Planck. C'est l'équation fondamentale qui connecte les deux mondes.
3. Interférences d'Young (Aspect Onde) :
Quand une onde (lumineuse ou de matière) passe par deux fentes, elle interfère avec elle-même. Sur un écran lointain, on observe des franges brillantes (interférences constructives) et sombres. Pour une longueur d'onde \(\lambda\), des fentes séparées de \(d\) et un écran à distance \(L\), l'écart entre deux franges brillantes (l'interfrange) est :
\[ \Delta y = \frac{\lambda \cdot L}{d} \]
Observer ce phénomène avec des électrons prouve leur nature ondulatoire.
Correction : Analyse de la Dualité Onde-Particule
Question 1 : Calculer la quantité de mouvement (p)
Principe (le concept physique)
La première étape consiste à traduire l'énergie de l'électron, donnée dans une unité pratique pour les physiciens (l'électron-volt, eV), en unité du Système International (le Joule). Une fois cette conversion faite, on peut utiliser la relation classique entre l'énergie cinétique et la quantité de mouvement pour quantifier l'aspect "particule" de l'électron : sa "quantité de mouvement".
Mini-Cours (approfondissement théorique)
L'électron-volt (eV) est une unité d'énergie définie comme l'énergie acquise par un électron accéléré par une différence de potentiel de 1 Volt. C'est une unité très adaptée à l'échelle atomique. La conversion est simple : \(1 \, \text{eV} = 1.602 \times 10^{-19} \, \text{J}\). La relation \(p = \sqrt{2mE_c}\) est non-relativiste. Pour des énergies beaucoup plus élevées (proches de \(m_e c^2\)), il faudrait utiliser la formule relativiste \(E^2 = (pc)^2 + (m_e c^2)^2\).
Remarque Pédagogique (le conseil du professeur)
Pensez à la quantité de mouvement comme à "l'inertie en mouvement" de la particule. C'est une mesure de la difficulté à l'arrêter. Même si l'électron est incroyablement léger, son énergie cinétique lui confère une quantité de mouvement bien réelle, qui est la clé pour débloquer son côté ondulatoire.
Normes (la référence réglementaire)
Il n'y a pas de "norme" au sens industriel, mais les valeurs des constantes fondamentales (masse de l'électron, charge, constante de Planck) sont standardisées et maintenues par des organismes internationaux comme le CODATA (Committee on Data for Science and Technology) pour assurer la cohérence des calculs scientifiques dans le monde entier.
Formule(s) (l'outil mathématique)
1. Conversion d'énergie :
2. Quantité de mouvement :
Hypothèses (le cadre du calcul)
On suppose que la vitesse de l'électron est suffisamment faible pour que les effets relativistes soient négligeables. L'énergie de 150 eV est bien inférieure à l'énergie de masse de l'électron (\(\approx 511 \, \text{keV}\)), donc l'approximation est excellente.
Donnée(s) (les chiffres d'entrée)
- Énergie cinétique, \(E_c = 150 \, \text{eV}\)
- Masse de l'électron, \(m_e = 9.11 \times 10^{-31} \, \text{kg}\)
- Charge élémentaire, \(e = 1.602 \times 10^{-19} \, \text{C}\)
Astuces(Pour aller plus vite)
Pour éviter les erreurs de calcul avec les puissances de 10, il est conseillé de traiter les nombres et les puissances séparément sur votre calculatrice ou brouillon. Assurez-vous que toutes les unités sont dans le Système International (m, kg, s, J) avant d'appliquer les formules finales.
Schéma (Avant les calculs)
De l'Énergie à la Quantité de Mouvement
Calcul(s) (l'application numérique)
1. Conversion de l'énergie en Joules :
2. Calcul de la quantité de mouvement :
Schéma (Après les calculs)
Résultat du Calcul de p
Réflexions (l'interprétation du résultat)
Cette valeur de \(p\) représente la "force de frappe" de notre particule. C'est une quantité extrêmement faible, comme attendu pour un objet subatomique, mais elle est non nulle et parfaitement définie. C'est cette quantité de mouvement qui va maintenant nous servir de pont pour explorer le comportement ondulatoire de l'électron.
Points de vigilance (les erreurs à éviter)
L'erreur la plus commune est d'oublier de convertir les électron-volts en Joules. Si vous utilisez directement 150 dans la formule de \(p\), le résultat sera complètement faux. La cohérence des unités du Système International est la clé.
Points à retenir (permettre a l'apprenant de maitriser la question)
- Toujours convertir les unités (comme l'eV) en unités du Système International (Joule) pour les calculs.
- La quantité de mouvement \(p\) est liée à l'énergie cinétique \(E_c\) par la formule \(p = \sqrt{2mE_c}\) en mécanique non-relativiste.
Le saviez-vous ? (la culture de l'ingénieur)
La quantité de mouvement est une quantité conservée, ce qui en fait l'une des grandeurs les plus fondamentales en physique. Dans les accélérateurs de particules, c'est la quantité de mouvement (et non la vitesse) qui est la variable la plus pertinente pour décrire les collisions.
FAQ (pour lever les doutes)
Résultat Final (la conclusion chiffrée)
A vous de jouer(pour verifier la comprehension de l'etudiant parrapport a la question)
Quelle serait la quantité de mouvement (en \(10^{-24} \, \text{kg} \cdot \text{m}/\text{s}\)) pour un électron avec une énergie de 300 eV ?
Question 2 : Calculer la longueur d'onde de De Broglie (\(\lambda\))
Principe (le concept physique)
Ici, nous franchissons le pas conceptuel majeur de la physique quantique. Grâce à l'hypothèse de Louis de Broglie, nous allons associer une propriété purement ondulatoire, une longueur d'onde, à notre électron, que nous traitions jusqu'à présent comme une particule. La formule est une simple division, mais son implication est profonde : tout ce qui a une quantité de mouvement a une longueur d'onde.
Mini-Cours (approfondissement théorique)
L'onde de De Broglie n'est pas une onde électromagnétique comme la lumière. C'est une "onde de probabilité". L'amplitude de cette onde au carré en un point de l'espace est proportionnelle à la probabilité de trouver la particule à cet endroit. Les interférences observées sont donc des interférences de probabilités : les électrons ont plus de chances d'arriver sur les franges brillantes.
Remarque Pédagogique (le conseil du professeur)
La relation \(\lambda = h/p\) est un magnifique exemple de la beauté et de la simplicité des lois fondamentales de la physique. Elle relie deux mondes apparemment incompatibles (ondes et particules) via une constante universelle, \(h\). C'est le pont conceptuel qui permet de passer de la description corpusculaire à la description ondulatoire.
Normes (la référence réglementaire)
La relation de De Broglie est une loi fondamentale de la nature, pas une norme technique. Cependant, ses applications, comme la microscopie électronique ou la diffraction de neutrons, sont régies par des protocoles et des standards expérimentaux très stricts pour garantir la fiabilité des mesures.
Formule(s) (l'outil mathématique)
Hypothèses (le cadre du calcul)
La formule est universelle et s'applique à toute particule. Aucune nouvelle hypothèse n'est nécessaire, si ce n'est d'accepter le postulat de De Broglie lui-même.
Donnée(s) (les chiffres d'entrée)
- Quantité de mouvement, \(p \approx 6.617 \times 10^{-24} \, \text{kg} \cdot \text{m}/\text{s}\) (de Q1)
- Constante de Planck, \(h = 6.626 \times 10^{-34} \, \text{J} \cdot \text{s}\)
Astuces(Pour aller plus vite)
Notez que la quantité de mouvement calculée (\(6.617 \times 10^{-24}\)) est très proche de la constante de Planck (\(6.626 \times 10^{-34}\)) à un facteur \(10^{10}\) près. Le calcul de \(\lambda\) sera donc très proche de \(10^{-10} \, \text{m}\). Repérer ces coïncidences numériques peut servir de vérification rapide.
Schéma (Avant les calculs)
Le Pont de De Broglie
Calcul(s) (l'application numérique)
On applique directement la formule de De Broglie.
Cette valeur est plus commodément exprimée en nanomètres (nm).
Schéma (Après les calculs)
Onde de Matière Associée
Réflexions (l'interprétation du résultat)
La longueur d'onde de l'électron est de 0.1 nm, soit 1 Angström. C'est un ordre de grandeur typique pour les distances interatomiques dans les cristaux. Ce n'est pas une coïncidence : c'est précisément parce que leur longueur d'onde est de cet ordre que les électrons peuvent être utilisés en diffraction (comme les rayons X) pour étudier la structure de la matière.
Points de vigilance (les erreurs à éviter)
Ne pas confondre l'onde de matière avec une onde électromagnétique (photon). Un électron a une masse et une charge, un photon n'en a pas. Leurs ondes respectives décrivent des phénomènes différents, même si les deux peuvent interférer.
Points à retenir (permettre a l'apprenant de maitriser la question)
- Toute particule de quantité de mouvement \(p\) a une longueur d'onde \(\lambda = h/p\).
- Plus la particule va vite (plus \(p\) est grand), plus sa longueur d'onde est courte.
Le saviez-vous ? (la culture de l'ingénieur)
Le microscope électronique fonctionne grâce à ce principe. En accélérant très fortement les électrons, on peut obtenir des longueurs d'onde beaucoup plus courtes que celles de la lumière visible, ce qui permet d'atteindre des résolutions bien plus élevées et de "voir" des objets de la taille d'un atome.
FAQ (pour lever les doutes)
Résultat Final (la conclusion chiffrée)
A vous de jouer(pour verifier la comprehension de l'etudiant parrapport a la question)
Quelle serait la longueur d'onde \(\lambda\) (en nm) pour l'électron de 300 eV de la question précédente (\(p \approx 9.36 \times 10^{-24} \, \text{kg} \cdot \text{m}/\text{s}\)) ?
Question 3 : Calculer l'interfrange (\(\Delta y\))
Principe (le concept physique)
Maintenant que nous connaissons la longueur d'onde de notre "onde de matière", nous pouvons la traiter comme une onde lumineuse dans une expérience d'optique classique. La figure d'interférence observée sur l'écran est la preuve tangible de la nature ondulatoire de l'électron. Nous allons calculer la distance caractéristique de cette figure : l'espacement entre deux maxima d'intensité (les franges brillantes).
Mini-Cours (approfondissement théorique)
La formule \(\Delta y = \lambda L/d\) est une approximation valable pour de petits angles de diffraction, c'est-à-dire quand la distance à l'écran \(L\) est beaucoup plus grande que l'écartement des fentes \(d\). Dans notre cas, \(L=1\) m et \(d=50\) µm, donc la condition \(L \gg d\) est largement satisfaite, ce qui valide l'utilisation de cette formule simple.
Remarque Pédagogique (le conseil du professeur)
Cette étape est cruciale : elle connecte le monde invisible de la longueur d'onde quantique (\(\lambda\), de l'ordre de 10-10 m) à une distance macroscopique et mesurable (\(\Delta y\), de l'ordre de 10-6 m). C'est ce lien entre la théorie et une observation concrète qui rend la physique si puissante.
Normes (la référence réglementaire)
Les techniques d'interférométrie, qu'elles soient optiques ou électroniques, sont utilisées dans de nombreux domaines de haute technologie (gravure de circuits intégrés, métrologie de précision). Les procédures pour ces mesures sont standardisées pour assurer leur reproductibilité et leur exactitude.
Formule(s) (l'outil mathématique)
Hypothèses (le cadre du calcul)
On utilise l'approximation des petits angles, justifiée par le fait que \(L \gg d\). On suppose également que les fentes sont infiniment fines (fentes d'Young idéales), ce qui en pratique n'est pas le cas et peut moduler l'intensité des franges (phénomène de diffraction).
Donnée(s) (les chiffres d'entrée)
- Longueur d'onde, \(\lambda \approx 1.001 \times 10^{-10} \, \text{m}\) (de Q2)
- Distance fentes-écran, \(L = 1.0 \, \text{m}\)
- Écartement des fentes, \(d = 50 \, \mu\text{m} = 50 \times 10^{-6} \, \text{m}\)
Astuces(Pour aller plus vite)
Pour évaluer l'ordre de grandeur, on peut faire un calcul mental : \(\lambda \approx 10^{-10}\), \(L=1\), \(d \approx 5 \times 10^{-5}\). Le résultat sera de l'ordre de \(10^{-10} / (5 \times 10^{-5}) = 0.2 \times 10^{-5} = 2 \times 10^{-6}\) m, soit 2 µm. Cela permet de vérifier rapidement le résultat de la calculatrice.
Schéma (Avant les calculs)
Géométrie de l'Interférence
Calcul(s) (l'application numérique)
Exprimons ce résultat dans une unité plus parlante, le micromètre (\(\mu\text{m}\)).
Schéma (Après les calculs)
Figure d'Interférence sur l'Écran
Réflexions (l'interprétation du résultat)
L'espacement prédit entre les franges est de 2 micromètres. C'est une distance très petite, mais mesurable avec des détecteurs modernes. Le fait que l'on puisse calculer cette distance à partir de l'énergie initiale de l'électron est un succès spectaculaire de la théorie quantique. Cela montre que même si les électrons sont envoyés un par un, chaque électron "interfère avec lui-même" comme s'il passait par les deux fentes à la fois, un concept au cœur du mystère quantique.
Points de vigilance (les erreurs à éviter)
Attention aux unités ! La distance \(d\) est donnée en micromètres (\(\mu\text{m}\)). Il est impératif de la convertir en mètres pour être cohérent avec les autres unités (L et \(\lambda\)). Une erreur ici conduirait à un résultat faux d'un facteur un million.
Points à retenir (permettre a l'apprenant de maitriser la question)
- L'interfrange \(\Delta y\) est la distance entre deux maxima d'intensité.
- Elle est proportionnelle à la longueur d'onde \(\lambda\) et à la distance à l'écran \(L\).
- Elle est inversement proportionnelle à l'écartement des fentes \(d\).
Le saviez-vous ? (la culture de l'ingénieur)
L'interférométrie est utilisée dans les télescopes pour combiner la lumière de plusieurs miroirs distants. En faisant interférer les ondes lumineuses, les astronomes peuvent synthétiser un télescope virtuel de la taille de l'écartement entre les miroirs, atteignant des résolutions phénoménales, capables de voir des détails sur des étoiles lointaines.
FAQ (pour lever les doutes)
Résultat Final (la conclusion chiffrée)
A vous de jouer(pour verifier la comprehension de l'etudiant parrapport a la question)
Si on utilisait des fentes plus larges, espacées de \(d = 100\) µm, quel serait le nouvel interfrange \(\Delta y\) en µm ?
Question 4 : Calculer l'angle de la première frange brillante (\(\theta_1\))
Principe (le concept physique)
Les franges brillantes apparaissent aux endroits où la différence de chemin parcouru par l'onde depuis chaque fente est un multiple entier de la longueur d'onde (\(\delta = k\lambda\)). Ce calcul nous permet de déterminer la direction dans laquelle on trouve le premier maximum d'interférence constructive, une autre façon de caractériser la figure d'interférence.
Mini-Cours (approfondissement théorique)
La relation \(d \sin(\theta_k) = k \lambda\) est la condition générale pour l'interférence constructive de deux sources ponctuelles. Pour \(k=0\), \(\theta_0=0\), c'est la frange centrale. Pour \(k=1\), on a la première frange brillante de chaque côté. Pour les franges sombres (interférence destructive), la condition est \(d \sin(\theta_k) = (k+1/2) \lambda\).
Remarque Pédagogique (le conseil du professeur)
Calculer l'angle est une approche plus fondamentale que de calculer l'interfrange, car l'angle ne dépend que de la physique du phénomène (\(\lambda\)) et de la géométrie des fentes (\(d\)), et non de la position de l'écran (\(L\)). C'est la signature angulaire de la diffraction.
Normes (la référence réglementaire)
En cristallographie par diffraction des rayons X ou d'électrons, c'est la loi de Bragg (\(2d\sin\theta = n\lambda\)) qui est utilisée. Elle est conceptuellement très proche de la formule des fentes d'Young et relie les angles de diffraction aux distances entre les plans atomiques dans un cristal.
Formule(s) (l'outil mathématique)
La condition pour une frange brillante est :
Pour la première frange, k=1 :
Hypothèses (le cadre du calcul)
Les mêmes hypothèses que pour la question 3 s'appliquent. La validité de la formule repose sur un modèle d'ondes planes arrivant sur les fentes.
Donnée(s) (les chiffres d'entrée)
- Longueur d'onde, \(\lambda \approx 1.001 \times 10^{-10} \, \text{m}\) (de Q2)
- Écartement des fentes, \(d = 50 \times 10^{-6} \, \text{m}\)
Astuces(Pour aller plus vite)
Pour des angles très petits, ce qui est presque toujours le cas dans ces expériences, on peut utiliser l'approximation \(\sin(\theta) \approx \theta\) (avec \(\theta\) en radians). Cela simplifie grandement le calcul : \(\theta_1 \approx \lambda/d\). Vous pouvez vérifier que \(\arcsin(x) \approx x\) pour de très petites valeurs de \(x\).
Schéma (Avant les calculs)
Angle de Diffraction
Calcul(s) (l'application numérique)
Comme la valeur du sinus est très petite, l'angle \(\theta_1\) sera très petit. On peut utiliser l'approximation \(\sin(\theta) \approx \theta\) pour \(\theta\) en radians.
Convertissons en degrés :
Schéma (Après les calculs)
Angle de la Première Frange Brillante
Réflexions (l'interprétation du résultat)
L'angle est extrêmement petit, ce qui justifie a posteriori l'utilisation de l'approximation des petits angles (\(\sin\theta \approx \tan\theta \approx \theta\)) qui est souvent faite pour dériver la formule de l'interfrange \(\Delta y = \lambda L/d\). Cet angle minuscule montre à quel point l'expérience est délicate à réaliser et à mesurer.
Points de vigilance (les erreurs à éviter)
Assurez-vous que votre calculatrice est en mode "radians" si vous utilisez l'approximation \(\theta \approx \lambda/d\), ou en mode "degrés" si vous calculez l'arcsinus puis convertissez. Une confusion entre les deux unités d'angle est une erreur fréquente.
Points à retenir (permettre a l'apprenant de maitriser la question)
- La direction des franges brillantes est donnée par \(d \sin(\theta_k) = k \lambda\).
- Pour de petits angles, on a \(\theta_k \approx k\lambda/d\) en radians.
- L'angle ne dépend pas de la distance à l'écran \(L\).
Le saviez-vous ? (la culture de l'ingénieur)
Les réseaux de diffraction, utilisés dans les spectromètres, sont constitués de milliers de fentes très rapprochées. Ils fonctionnent sur le même principe, mais en utilisant un grand nombre de fentes, les pics d'interférence deviennent extrêmement fins et brillants, ce qui permet de séparer les différentes longueurs d'onde (couleurs) de la lumière avec une très grande précision.
FAQ (pour lever les doutes)
Résultat Final (la conclusion chiffrée)
A vous de jouer(pour verifier la comprehension de l'etudiant parrapport a la question)
Quel serait l'angle \(\theta_1\) en microradians (µrad) si on utilisait des fentes espacées de \(d = 25\) µm ?
Outil Interactif : Paramètres d'Interférence
Modifiez les paramètres de l'expérience pour voir leur influence sur la figure d'interférence.
Paramètres d'Entrée
Résultats Clés
Le Saviez-Vous ?
Louis de Broglie a présenté son hypothèse révolutionnaire sur les ondes de matière dans sa thèse de doctorat en 1924. Le jury, perplexe, a demandé l'avis d'Albert Einstein. Ce dernier, reconnaissant immédiatement la profondeur de l'idée, a répondu que c'était le premier rayon de lumière sur le plus grand des mystères de la physique. De Broglie a reçu le prix Nobel pour cette idée seulement cinq ans plus tard, en 1929.
Foire Aux Questions (FAQ)
Est-ce que les objets macroscopiques comme une balle de tennis ont aussi une longueur d'onde ?
Oui, absolument ! Tout objet avec une quantité de mouvement en a une. Cependant, à cause de la constante de Planck \(h\) qui est minuscule, et de la masse (et donc de la quantité de mouvement) qui est énorme pour un objet macroscopique, la longueur d'onde est extraordinairement petite (de l'ordre de 10-34 m pour une balle de tennis), la rendant totalement indétectable en pratique. Les effets ondulatoires ne sont visibles que pour les particules subatomiques.
Que se passe-t-il si on essaie de savoir par quelle fente l'électron passe ?
C'est le cœur du paradoxe quantique. Si vous placez un détecteur près d'une des fentes pour "observer" le passage de l'électron, la figure d'interférence disparaît ! L'acte de mesure force l'électron à se comporter comme une particule localisée, et il ne passe que par une seule fente. On obtient alors deux bandes sur l'écran, comme si on lançait des billes. C'est ce qu'on appelle "l'effondrement de la fonction d'onde".
Quiz Final : Testez vos connaissances
1. Si on double l'énergie cinétique d'un électron, sa longueur d'onde de De Broglie est...
2. Pour obtenir des franges d'interférence plus espacées sur l'écran, il faut...
- Dualité Onde-Particule
- Concept central de la mécanique quantique selon lequel les objets peuvent manifester des propriétés à la fois d'ondes (interférence, diffraction) et de particules (position, quantité de mouvement).
- Longueur d'onde de De Broglie (\(\lambda\))
- Longueur d'onde associée à toute particule en mouvement, reliant son aspect ondulatoire à son aspect corpusculaire via la relation \(\lambda = h/p\).
- Interférence
- Phénomène qui se produit lorsque deux ou plusieurs ondes se superposent. L'amplitude résultante peut être plus grande (constructive) ou plus petite (destructive) que celle des ondes individuelles.
D’autres exercices de physique quantique:

0 commentaires